Безопасность медицинских изделий и управление риском
Безопасность можно рассматривать только в относительном выражении. Все изделия характеризуются определенной степенью риска и при определенных обстоятельствах могут способствовать возникновению проблем. Многие из таких проблем нельзя обнаружить до тех пор, пока на рынке не будет накоплен обширный опыт. Например, имплантируемое изделие может дать сбой, который невозможно было предсказать в момент имплантации; этот сбой может отражать условия, специфические для определенных пациентов. В других изделиях возможен непрогнозируемый или случайный выход из строя какого-либо компонента. Нынешний подход к безопасности изделий заключается в оценке потенциальной угрозы, которую может представлять изделие и, которая способна привести к проблемам с безопасностью и нанесению вреда. Эту оценку часто называют оценкой рисков.
Безопасность и функциональные характеристики медицинских изделий
Изделие является клинически эффективным, если позволяет получить предусмотренный изготовителем эффект относительно конкретного медицинского состояния. Клиническая эффективность является хорошим показателем функциональных характеристик изделия. При этом, помимо клинической эффективности данные характеристики могут включать и технические функции. Например, функция сигнализации не влияет напрямую на клиническую эффективность, однако служит другим полезным целям. Более того, по сравнению с клинической эффективностью, функциональные характеристики легче поддаются объективному измерению и количественному выражению. Они тесно связаны с безопасностью. Например, шприц для взятия крови с тупой иглой будет малопригоден для забора крови и может нанести травму. Плохо работающий прибор для контроля за состоянием пациента чреват серьезными проблемами для клинической безопасности последнего. Поэтому безопасность и функциональные характеристики медицинских изделий обычно рассматриваются вместе.
Этапы периода жизни медицинского изделия
На рис. 1 отображены основные этапы периода жизни медицинского изделия - от формирования его концепции и разработки - до утилизации. Активные этапы представлены в упрощенной форме, чтобы облегчить понимание системы регулирования. Например, этап разработки охватывает планирование разработки, верификацию/валидацию конструкции, испытания прототипа и клинические испытания. На практике между приведенными здесь этапами возможно частичное совпадение и взаимодействие.
Обеспечение безопасности медицинских изделий
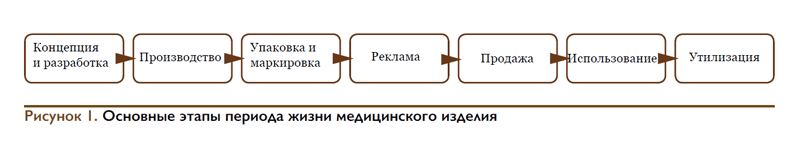
Как следует из рис. 2, «изготовитель» обычно руководит первыми тремя этапами периода жизни медицинского изделия. Под термином «организация (учреждение)» подразумеваются импортеры, дистрибьюторы, розничные торговцы и изготовители, которые реализуют медицинское изделие на рынке. «Пользователь» – это специалист медицинского учреждения или также пациент.
Все они – изготовитель, организации (учреждения), пользователь, общественность и национальный регуляторный орган / органы власти выступают заинтересованными сторонами. Каждая играет крайне важную роль в обеспечении безопасности медицинских изделий. Самым важным фактором, составляющим основу для сотрудничества между всеми пятью заинтересованными сторонами, является глубокое единое понимание соответствующей проблематики. Общее понимание и ответственность формируется посредством коммуникации и взаимного просвещения, чего можно с успехом достичь путем вовлечения всех заинтересованных сторон в разработку процесса, призванного гарантировать безопасность и функциональные характеристики медицинских изделий.